转自:药明康德
根据PDUFA的预期目标日期,预计2025年4月,美国FDA将对4款创新药物的批准做出监管决定,本文将对这些疗法进行相关介绍。
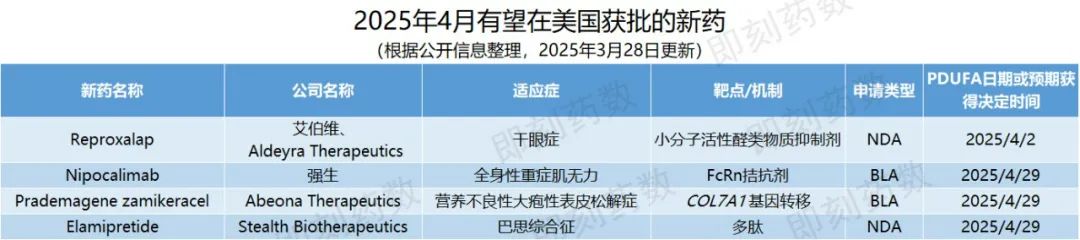
活性成分:Reproxalap
适应症:干眼症(DED)
公司名称:艾伯维(AbbVie)、AldeyraTherapeutics

Reproxalap是一款潜在“first-in-class”的在研小分子活性醛抑制剂。活性醛含量会在眼部或系统性发炎时上升,造成眼睛发炎、泪水分泌降低、眼睛发红以及改变泪水内脂质组成,许多干眼症患者具有较高的活性醛含量。
去年8月,该公司宣布reproxalap在一项随机双盲、载体对照的3期临床试验中达到主要终点,在改善眼部不适的主要终点方面,reproxalap在统计学上显著优于载体(P=0.004)。在这项3期临床试验中,患者在进入干眼室(dryeyechamber,一个让患者更容易出现干眼症状的不良环境)前被给予载体(不含有效成分的药品),符合试验标准的患者随后被随机分配进入试验下一阶段,在进入干眼室前接受reproxalap或载体。在随机分配的132名患者中,66名患者接受了reproxalap治疗,66名患者接受了载体。主要终点是在干眼室中从80到100分钟的眼部不适。试验结果显示接受reproxalap治疗的患者眼部不适显著降低。
活性成分:Nipocalimab
适应症:全身性重症肌无力(gMG)
公司名称:强生(Johnson&Johnson)

Nipocalimab是一款潜在“best-in-class”,靶向新生儿Fc受体的抗体疗法。已在临床试验中显示可降低免疫球蛋白(IgG)水平,包括致病性IgG,这被认为是自身抗体疾病的根本原因之一。这款疗法被行业媒体Evaluate列为今年有望上市的10大潜在重磅疗法之一。

该疗法用以治疗gMG患者的3期研究数据显示,研究达到主要终点,在24周内,接受nipocalimab治疗患者的gMG疾病指标日常生活活动评分(MG-ADL)获得统计学显著和具有临床意义的改善。此外,nipocalimab可使患者的总IgG的中位水平与基线相较降低最多达75%。此外,研究还观察到常见的致病性IgG(如抗AChR抗体和抗MuSK抗体)水平在24周内显著下降。研究未观察到总IgE、IgA和IgM的变化,这表明即使在致病性IgG自身抗体水平下降后,保护性免疫系统仍可能保持正常功能。
活性成分:prademagenezamikeracel
适应症:营养不良性大疱性表皮松解症
公司名称:AbeonaTherapeutics

Prademagenezamikeracel(pz-cel)是AbeonaTherapeutics公司开发的一款基因疗法,旨在将功能性、产生胶原的COL7A1转基因递送到患者自身的皮肤细胞中,并通过使用逆转录病毒载体稳定整合到分裂的靶细胞DNA中,实现长期基因表达。
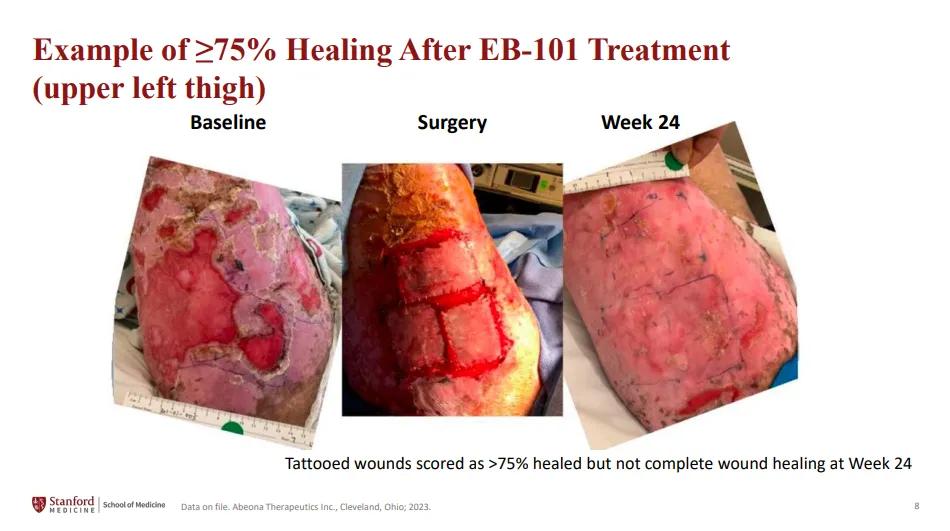
该上市申请主要获得关键性3期临床试验VIITAL以及另一项1/2a期研究的临床疗效和安全性数据支持。两项研究均显示,在大型和慢性伤口上单次应用pz-cel治疗可实现持续伤口愈合和疼痛减轻。分析显示,该疗法在VIITAL试验中达成两项主要终点,大多数(81%)pz-cel治疗的伤口显示出≥50%的愈合程度,并且与对照伤口相比,pz-cel治疗的伤口中观察到疼痛严重程度有更大程度的减轻。即使在较早的时间点,与对照伤口相比,使用pz-cel治疗的伤口显示愈合的百分比和疼痛严重程度的降低也更大。
活性成分:Elamipretide
适应症:巴思综合征(Barthsyndrome)
公司名称:StealthBiotherapeutics

Elamipretide是一种肽化合物,可轻易穿透细胞膜,靶向线粒体内膜,并可逆性地与心磷脂(cardiolipin)结合。在临床前或临床研究中观察到该疗法可增加线粒体呼吸作用、改善电子递送链功能和ATP生成,并减少致病性活性氧(ROS)的形成。这种elamipretide-心磷脂结合已被证明可以使线粒体内膜结构正常化,从而改善线粒体功能。2024年10月,美国FDA心血管和肾脏药物咨询委员会(CRDAC)以10比6的票数支持StealthBiotherapeutics的在研疗法elamipretide用于治疗巴思综合征患者。根据新闻稿,如果获得批准,elamipretide将成为巴思综合征的首款获批疗法。
临床2/3期试验结果显示,elamipretide每日治疗显示出改善巴思综合征症状的潜力。研究首先进行了一项随机、双盲、安慰剂对照交叉试验,随后开展开放标签扩展试验,以评估其疗效和安全性。在第一部分试验中,12名受试者被随机分配接受每天40mg的elamipretide或安慰剂治疗,为期12周,在经过为期4周的药物洗脱期后,进行为期12周的安慰剂治疗。然而,这一阶段未能达到两个主要终点。
在第二部分开放标签扩展阶段,10名受试者继续接受每天40mg的elamipretide治疗,8名受试者完成了36周治疗。结果显示显著改善:6分钟步行测试(6MWT)平均增加95.9米(p=0.024),巴思综合征症状评估量表(BTHS-SA)平均降低2.1分(p=0.031)。此外,膝关节伸肌力量、患者整体症状印象和部分心脏参数等次要终点也有明显改善。总体而言,尽管第一阶段未达主要终点,但第二阶段的长期治疗结果表明,elamipretide对改善巴思综合征症状具有潜在疗效。
参考资料:
[1]AldeyraTherapeuticsAnnouncesFDAAcceptanceforReviewofReproxalapNewDrugApplicationfortheTreatmentofDryEyeDisease,ExpandsAbbVieOptionAgreemen.RetrievedNovember18,2024fromhttps://www.businesswire.com/news/home/20241118246408/en
[2]FindingsfrompivotalnipocalimabPhase3studyinabroadantibodypositivepopulationofpeoplelivingwithgeneralisedmyastheniagravispublishedinTheLancetNeurology.RetrievedJanuary23,2025,fromhttps://www.globenewswire.com/news-release/2025/01/23/3014089/0/en/Findings-from-pivotal-nipocalimab-Phase-3-study-in-a-broad-antibody-positive-population-of-people-living-with-generalised-myasthenia-gravis-published-in-The-Lancet-Neurology.html
[4]StealthBioTherapeuticsAnnouncesPositiveVotefromFDAAdvisoryCommitteeMeetingSupportingPotentialApprovalofElamipretidefortheTreatmentofBarthSyndrome.RetrievedDecember26,2024fromhttps://stealthbt.com/stealth-biotherapeutics-announces-positive-vote-from-fda-advisory-committee-meeting-supporting-potential-approval-of-elamipretide-for-the-treatment-of-barth-syndrome/
